超高齢社会を迎えたわが国において、「国民の長寿」と「質の高い生活」を実現するためには、新しい医療機器・再生医療等製品の開発と医療現場への円滑な導入が不可欠です。この分野の活性化・国際競争力の強化を図り、迅速な開発と審査を実現し、また、産業の育成の観点から、医療機器・再生医療等製品及びこれらに関連する研究開発の指針を明確化することが必要と考えます。
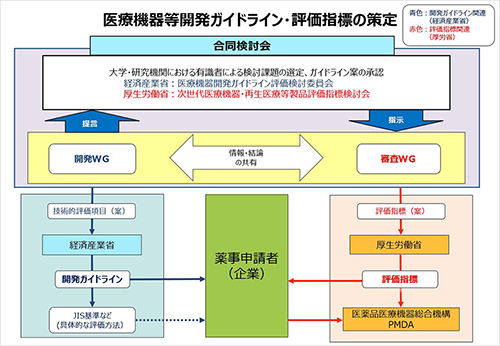
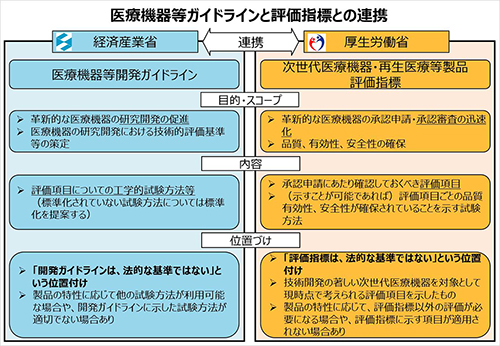
これらの目的のために、平成17年度から経済産業省に「医療機器開発ガイドライン評価検討委員会」と厚生労働省に「次世代医療機器・再生医療等製品評価指標検討会」が設置[PDF:87KB]され、以降、これらの検討会の連携(合同検討会)によって、新しい医療機器等の開発促進及び迅速な薬事承認審査に活用できる開発ガイダンス及び評価指標が策定されております。
開始から15年を経て医療機器産業を取り巻く情勢も変化したことから、開発ガイダンスの目的、策定プロセスの大幅見直しを行いました。令和5年度から新規に策定する文書につき「医療機器開発ガイダンス」に呼称を変更しました。ガイダンス文書の目的を4類型に分類し、テーマ選定・策定プロセスの透明化を図っていきます。
- 医療機器開発ガイドライン策定事業における前捌き機能と自立化に関する業務報告書
(2023/3 株式会社ドゥリサーチ研究所・AMED) - 医療機器開発ガイドライン(手引き)のためのガイドライン策定調査報告書
(2023/3 株式会社ドゥリサーチ研究所・AMED) - 「医療機器開発ガイドラインの今後のあり方に関する調査」 調査報告書
(2022/3 株式会社ドゥリサーチ研究所・AMED)
これまで策定した医療機器開発ガイダンスは経済産業省のホームページをご参照ください。機器の開発、薬事申請などにご活用ください。
厚生労働省の「次世代医療機器・再生医療等製品評価指標検討会」において、迅速な審査に必要な評価指標に関して検討がなされております。国立医薬品食品衛生研究所が事務局となり、審査ワーキンググループを設置して審査の迅速化という観点から種々の検討が進められております。同研究所のホームページに掲載される審査ワーキンググループの報告書(https://dmd.nihs.go.jp/jisedai/)も併せてご覧ください
関連リンク
- 日本医療研究開発機構 (https://www.amed.go.jp/)
- 経済産業省 (https://www.meti.go.jp/)
医療機器開発ガイダンス(METI/経済産業省)(https://www.meti.go.jp/policy/mono_info_service/healthcare/report_iryou_fukushi.html) - 厚生労働省 (https://www.mhlw.go.jp/)
- 国立医薬品食品衛生研究所 (https://www.nihs.go.jp/index-j.html)
審査ワーキンググループ報告書 (https://dmd.nihs.go.jp/jisedai/) - 独立行政法人 医薬品医療機器総合機構 (https://www.pmda.go.jp/)
- 日本医療機器産業連合会(医機連)(https://www.jfmda.gr.jp/)
- IMDRF(The International Medical Device Regulators Forum)(http://www.imdrf.org/)